O que é pH?
- Ciência povão

- 30 de set. de 2020
- 6 min de leitura
Saudações, meu querido povão! Tudo caminhando? Espero que sim, pois o importante é não estagnar. Hoje falaremos um pouco sobre uma sigla que muitos de vocês já devem ter escutado, ou observado em alguns locais, o pH. Mas afinal, o que é e para que a gente usa esse negócio? Vem com a gente!

Potencial Hidrogeniônico (pH)
Quando nos referimos a pH, estamos falando de Potencial Hidrogeniônico (que ‘diabé’ isso?). Basicamente, é uma escala de medida da acidez, neutralidade e/ou basicidade (alcalinidade) de um meio ou uma substância qualquer. Podemos medir o pH do solo, da água, do sangue, de alimentos, enfim, de uma gama de situações.
E o que seriam essas três categorias citadas acima? Quando estudamos química, aprendemos, bem no começo, o que são íons. Íons são átomos dotados de carga elétrica, e esta carga pode ser positiva (resultante da perda de um elétron), ou negativa (resultante do ganho de um elétron). Os íons positivos são denominados Cátions e, por sua vez, os negativos são chamados Ânions.

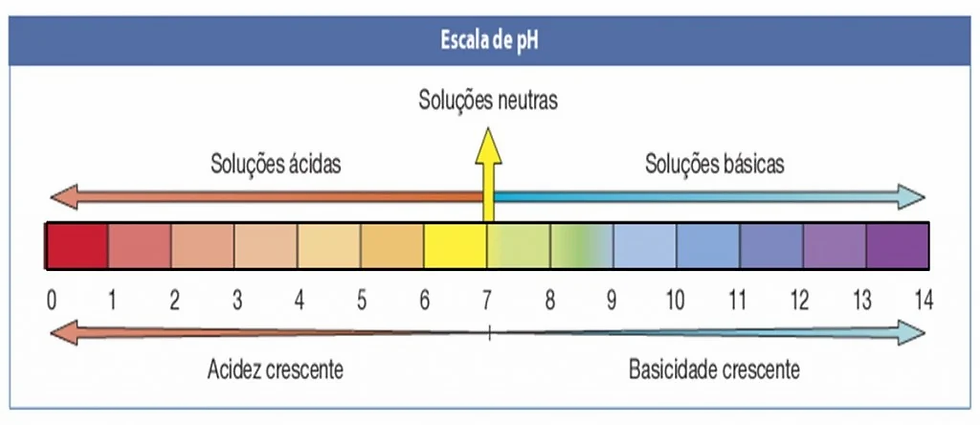
O pH leva em consideração a concentração de cátions H+ e ânions OH- presentes no meio, e as quantidades desses íons vão determinar se esse meio será ácido, neutro ou básico (alcalino). A medida é determinada por uma variação numérica que vai de 0 a 14*.
*esses valores são originados a partir de cálculos, que levam
em consideração o comportamento da água. Não nos aprofundaremos nisso
por não ser algo que interfira no entendimento geral*
• O meio será ácido caso a concentração de H+ seja maior que a de OH-
. O meio será neutro caso a concentração de H+ seja igual a de OH-
. O meio será básico (alcalino) caso a concentração de H+ seja menor que a de OH-
Por sua vez, quanto maior a concentração de H+, menor será o pH do meio ou da substância. Num primeiro momento podemos nos enganar pensando que um pH baixo significaria algo fraco ou ínfimo, devido ao seu baixo valor numérico, porém quanto mais baixo o pH, mais ácido será o meio, ao passo que quanto mais alto for o pH, mais básico será o meio. A escala numérica é dividida da seguinte forma:
. Se o pH for 7 (exatamente a metade da escala), temos um meio/substância neutra. O maior exemplo que temos é a água;
. Se o pH for abaixo de 7, temos um meio/substância ácida. Alguns ácidos comuns são o vinagre, refrigerantes, vitamina C, etc.
. Se o pH for acima de 7, temos um meio/substância básica. Produtos de limpeza, antiácidos e cal são alguns exemplos de substâncias básicas.
Para poder entender melhor, vamos considerar o valor 7 como ponto de partida. Caso o pH diminua de valor, o meio será mais ácido, logo, quanto mais se aproxima de zero, mais ácida vai ficando o meio; de modo semelhante, quanto mais o pH se aproxima de 14, mais básico vai ficando o meio. Substâncias muito ácidas ou muito básicas podem ser perigosas pelo seu poder corrosivo, como por exemplo o ácido sulfúrico (H2SO4) e a soda cáustica (NaOH), substância básica utilizada na limpeza de ralos.

Link do vídeo dos efeitos de alguns ácidos na carne de galinha: https://www.emsintese.com.br/2015/carne-de-galinha-em-acido-fluoridrico/
Com base nisso, também podemos modificar o pH de um meio através de uma correção, adicionando um ácido ou uma base. Como assim? Ácidos e bases são substâncias que podem reagir entre si e neutralizar o meio, ou seja, caso um meio/substância seja ácido/a, basta adicionar uma base a fim de ocorrer a neutralização. Do mesmo modo, podemos adicionar um ácido em um meio básico e provocar a neutralização.
Por que é importante saber isso? Aplicações do pH no dia-a-dia
Se prestarmos atenção, estamos cercados pelas ciências naturais no nosso dia-a-dia. A química está nos nossos produtos de higiene pessoal, de limpeza, nos medicamentos, nos alimentos, e por aí vai. O pH está presente em tudo isso, inclusive em nós mesmos.
Estômago
Nosso estômago produz ácido clorídrico (HCl), uma substância extremamente ácida, de modo que o meio estomacal trabalha em um pH em torno de 2.
Quando nos alimentamos e sentimos azia ou queimação na região estomacal, causada pelo refluxo do suco gástrico, podemos ingerir um antiácido para resolver o problema. Os antiácidos são substâncias básicas que servem para neutralizar a acidez da azia. Porém, a acidez excessiva no estômago pode causar problemas sérios como gastrite, que se não tratada, pode evoluir para uma úlcera.

Vagina
A vagina é um órgão que possui pH ácido, que varia de 3,8 - 4,5. Essa acidez é mantida com ajuda da microbiota vaginal, promovendo a proteção contra outros microrganismos que podem causar infecções. Variações no pH vaginal, causadas pelo desequilíbrio da microbiota vaginal, podem acarretar numa série de complicações causadas por fungos e bactérias invasoras.
Sangue
O nosso sangue trabalha em valores bem específicos de pH, que vão de 7,35 até 7,45. Ele é levemente básico, de acordo com a escala de pH, mas nesse caso as variações são tão sensíveis que qualquer valor abaixo de 7,35 já é considerado sangue ácido e, acima de 7,45, é considerado básico, sendo que ambas as situações podem levar o indivíduo à morte. O corpo sempre trabalha a fim de promover o equilíbrio do pH sanguíneo, mantendo-o na faixa de 7,35 - 7,45. Existem casos de mergulho de apneia (mergulho livre, sem utilização de equipamentos) em que o mergulhador realiza a hiperventilação (aquela respiração acelerada) para ficar mais tempo debaixo d’água. Isso realmente funciona, mas é bastante perigoso, pois o corpo percebe as variações do pH sanguíneo, que se torna mais ácido, e num movimento de reflexo, provoca involuntariamente os movimentos para respiração, provocando afogamento.

Outras aplicações
Na agricultura, utilizamos o pH para verificar solos ideais para o plantio. A sua composição, que pode conter sais, metais e outras substâncias, interfere no seu pH, deixando-o ácido ou básico. Algumas plantas têm preferência por solos levemente mais ácidos, como por exemplo o café, que cresce bem em solos com pH em torno de 5,2 - 6,3, enquanto outras têm preferência por solos básicos, como a uva.
Os produtos de higiene também são produzidos com alto controle do pH, como por exemplo os sabonetes, que possuem pH básico. Contudo, não pode ser básico em excesso, pois pode causar danos à pele.
Os rios Negro e Solimões são os rios que se unem para formar o Amazonas. O local do encontro das águas é um cenário magnífico, pois não há mistura (pelo menos não imediata). Isso é provocado principalmente pela diferença de densidade e temperatura, mas o pH das águas também é diferente. Águas negras geralmente possuem pH ácido, o rio Negro por exemplo possui pH em torno de 3,8 - 4,9, enquanto que as águas claras geralmente possuem pH básico.

Um grande problema que estamos provocando é a acidificação dos oceanos. Estamos aumentando muito as concentrações de CO2 na atmosfera, que acaba se difundindo até a água. Uma vez na água, o CO2 se dissolve formando o ácido carbônico, diminuindo o pH dos oceanos. Essa queda dos valores de pH torna indisponível os íons Carbonato nas águas, o que impede os organismos marinhos, como os corais, as algas e os mariscos, de produzirem suas estruturas corpóreas (que utilizam esse íon como matéria prima), resultando no enfraquecimento e, consequentemente, na morte desses organismos.

É isso minha gente! Espero que tenham gostado e que tenham entendido o que é ter um shampoo pH neutro. Boa semana a todos!

Autor
Membro do Ciência Povão
Adriano Lima
Biólogo
Referências
MENDES, M.D; SECO, M.A; BARBOSA, I.R; RIBEIRO, L.P.D. A IMPORTÂNCIA DO PH NO NOSSO DIA A DIA. In: Semana universitária. 2008.
ANTUNES, M.; ADAMATTI, DANIELA S.; PACHECO, M.A.R; GIOVANELA, M. PH DO SOLO: DETERMINAÇÃO COM INDICADORES ÁCIDO-BASE NO ENSINO MÉDIO. Química Nova Escola, Vol 31 (4). 2009
DIAS, Diogo Lopes. "Conceito de pH"; Brasil Escola. Disponível em: https://brasilescola.uol.com.br/quimica/conceito-ph.htm. Acesso em 28 de setembro de 2020.
Medeiros, Tainah. Como fazer a higiene íntima feminina. Disponível em: https://drauziovarella.uol.com.br/mulher-2/como-fazer-a-higiene-intima-feminina/. Acesso em: 28/09/2020
Gostaram? Continuem com a gente, pois estaremos sempre trazendo novidades para vocês. Nos sigam no instagram @cienciapovao. Aproveitem e compartilhem com amigos e familiares.




Comentários